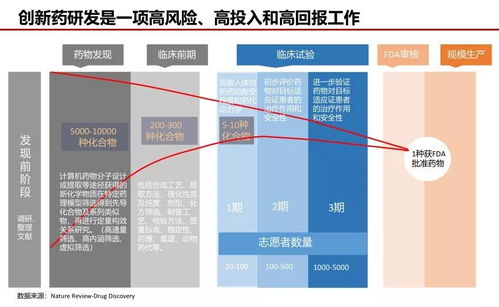
新藥研發是一項融合了尖端科學、嚴謹工程與巨大商業冒險的系統性工程。從最初的靈光一現到最終惠及患者,其歷程往往跨越數十年,耗資數十億美元,成功率卻微乎其微。這個過程不僅是科學與技術的長征,更是對人類耐心、智慧與資源的終極考驗。
第一階段:藥物發現與臨床前研究(約3-6年)
一切始于一個“靶點”——即與疾病相關的生物分子(如蛋白質、基因)。科學家通過基因組學、蛋白質組學等研究,識別出可能導致疾病的靶點。在數以萬計乃至百萬計的化合物庫中,通過高通量篩選、計算機輔助藥物設計等手段,尋找能夠與靶點相互作用并調節其功能的“先導化合物”。
獲得先導化合物后,便進入復雜的優化階段。藥物化學家對其進行反復的結構修飾與改造,旨在提升其效力、選擇性(只作用于靶點,減少副作用),并改善其“類藥性”,即藥物在人體內吸收、分布、代謝、排泄(ADME)的特性。毒理學家開始在細胞模型和動物模型(如小鼠、大鼠、犬類)中進行全面的藥效學、藥代動力學和安全性評估。這一階段的核心目標是得到一個在有效性和初步安全性上都表現優異的候選藥物,并為其申請進入人體臨床試驗。
第二階段:臨床試驗(約6-7年)
這是新藥研發中耗時最長、成本最高、風險最集中的環節,分為三期:
- I期臨床試驗:通常在少數(20-100名)健康志愿者或患者中進行。主要目的是評估藥物的安全性、耐受性,并初步了解其在人體內的代謝過程和藥理活性。此階段確定藥物的安全劑量范圍。
- II期臨床試驗:在數百名目標疾病患者中進行。重點在于評估藥物的有效性(是否對疾病有治療作用),并進一步觀察其安全性,為III期試驗的設計(如劑量、給藥方案)提供依據。此階段淘汰率極高。
- III期臨床試驗:在更大規模(數百至數千名)的患者群體中進行,采用隨機、雙盲、對照的嚴謹設計。這是確證性試驗,旨在全面評估藥物的有效性和安全性,充分了解其益處與風險比。成功通過III期試驗,是藥物獲批上市的關鍵基石。
第三階段:監管審批與上市(約1-2年)
完成所有臨床試驗后,研發企業需向監管機構(如美國FDA、中國NMPA)提交浩如煙海的申報資料,包括所有藥學、臨床前和臨床試驗數據。監管機構進行極其嚴格的審評,評估藥物的效益是否大于風險。這個過程可能要求企業補充數據或進行更多研究。最終獲批后,新藥方可正式上市銷售。
第四階段:上市后監測(IV期臨床試驗)
新藥上市并非終點。在真實世界的廣泛應用中,藥品需要在更大、更多樣化的人群中接受長期的安全性監測,以發現那些在前期臨床試驗中因樣本量有限而未能發現的罕見或長期不良反應。這是對患者安全持續負責的重要環節。
貫穿始終的挑戰與感嘆
縱觀全流程,新藥研發的“高風險”屬性無處不在:靶點驗證可能失敗,化合物可能無效或毒性太大,任何一期臨床試驗的負面結果都可能導致前功盡棄。統計顯示,平均每5000-10000個初始化合物中,最終只有一個能成功上市。其“高投入”同樣驚人,根據塔夫茨大學藥物開發研究中心的評估,成功研發一個新藥的平均成本已超過26億美元。
這數十年、數十億的“大工程”,匯聚了生物學、化學、醫學、統計學、數據科學、工程學等多學科頂尖人才的智慧與汗水。每一次成功上市的創新藥背后,都意味著對生命奧秘的又一次深刻理解,以及對人類健康福祉的一份堅實貢獻。在感嘆其艱辛與昂貴之余,我們更應對這份致力于攻克疾病、延長生命、提高生活質量的偉大事業,報以最高的敬意與期待。